Item 241 – Goitre
________________________________________________________________________
Situations de départ
- 17 Amaigrissement.
- 21 Asthénie.
- 24 Bouffées de chaleur.
- 25 Hypersudation.
- 148 Goitre ou nodule thyroïdien.
- 165 Palpitations.
- 194 Analyse du bilan thyroïdien.
- 225 Découverte d’une anomalie cervico-faciale à l’examen d’imagerie médicale.
- 284 Consultation de suivi et éducation thérapeutique d’un patient avec hypothyroïdie.
- 328 Annonce d’une maladie chronique.
- 352 Expliquer un traitement au patient (adulte, enfant, adolescent).
________________________________________________________________________________
________________________________________________________________________________
Hiérarchisation des connaissances
________________________________________________________________________________
| Rang | Rubrique | Intitulé | Descriptif |
| A | Définition | Définition du goitre | Définir un goitre et ses différents types |
| A | Examens complémentaires | Connaître l’indication des examens d’imagerie devant un goitre, des nodules | |
| B | Éléments physiopathologiques | Connaître les principaux facteurs favorisants de goitre, de nodules, de cancer | Iode, tabac, lithium… |
| A | Diagnostic positif | Connaître les trois principaux diagnostics étiologiques de goitres | Basedow, Hashimoto, thyroïdite subaiguë de De Quervain |
| A | Diagnostic positif | Connaître les trois principales complications évolutives d’un goitre | Hyperthyroïdie, compression, cancer |
| A | Examens complémentaires | Connaître les examens complémentaires à réaliser en première intention en présence d’un goitre | TSH, échographie… |
| A | Définition | Connaître la définition d’un nodule thyroïdien | |
| A | Diagnostic positif | Connaître les deux problématiques à résoudre en présence d’un nodule thyroïdien | Sécrétant ? Malin ? |
| A | Diagnostic positif | Connaître les éléments de l’interrogatoire et de l’examen clinique permettant la découverte et l’évaluation initiale d’un nodule | |
| A | Examens complémentaires | Connaître les examens complémentaires de première intention pour explorer un nodule thyroïdien | TSH, calcitonine |
| B | Examens complémentaires | Connaître la place de la cytologie dans la prise en charge d’un nodule thyroïdien | |
| B | Définition | Connaître les principaux types histologiques des cancers thyroïdiens | |
| B | Prise en charge | Connaître les principes de la prise en charge du goitre et des nodules (à l’exception du cancer) | Savoir ne pas prescrire d’opothérapie |
________________________________________________________________________________
Goitre
- Définition
- Epidémiologie
- Facteurs favorisants
- Démarche diagnostique
- Démarche étiologique
- Prise en charge thérapeutique
I Définition
On parle de goitre devant une augmentation du volume thyroïdien diffuse ou localisée (goitre nodulaire). Le volume thyroïdien normal varie suivant l’âge et la surface corporelle.
Les critères échographiques sont un volume thyroïdien > 16 ml chez l’adolescent, > 18 ml chez la femme et > 20 ml chez l’homme.
En pratique clinique, on convient de parler de goitre lorsqu’à la palpation la surface de chacun des lobes excède celle de la dernière phalange du pouce (définition OMS). L’existence d’un goitre ne préjuge pas du fonctionnement thyroïdien.
II Épidémiologie
Il s’agit d’une pathologie rencontrée chez plus de 10 % de la population, touchant 3 fois plus souvent les femmes que les hommes et dont la prévalence augmente avec l’âge (fig. 1).
III Facteurs favorisants
La déficience iodée, même relative, constitue le principal facteur goitrigène. Elle augmente, en effet, la sensibilité du parenchyme thyroïdien à l’effet trophique de la TSH et favorise aussi la production intrathyroïdienne de facteurs de croissance tissulaire. L’apport iodé optimal est de 100 à 150 μg par jour chez l’adulte. Chez la femme enceinte, il est de 200 à 250 μg par jour.
En France, l’apport iodé journalier, longtemps insuffisant, a été optimisé grâce à l’instauration d’une supplémentation en iode du sel de table (qui ne concerne pas la cuisine de collectivité : cantines, restaurants, plats cuisinés…) et à la diversification alimentaire.
Les apports journaliers en iode restent insuffisants chez la femme enceinte.
Une prédisposition familiale est souvent retrouvée. Plusieurs gènes de prédisposition ont été identifiés mais il s’agit d’une affection multigénique qui ne justifie pas de dépistage.
Les follicules thyroïdiens ont des récepteurs pour les œstrogènes : les goitres apparaissent en général à la puberté, augmentent pendant la grossesse et en cas de multiparité, surtout en cas de carence iodée.
Le tabac, qui contient notamment des thiocyanates, est goitrigène, mais n’augmente pas le risque de cancer thyroïdien.
Le lithium, qui se comporte comme un antithyroïdien de synthèse, peut favoriser la survenue d’un goitre.
________________________________________________________________________________
Fig. 1
Définition, facteurs de risque, épidémiologie des goitres.
(Source : CEEDMM, 2021.)

________________________________________________________________________________
IV Démarche diagnostique
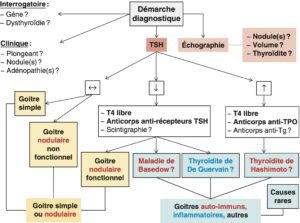
La démarche diagnostique est résumée dans la figure 2.
________________________________________________________________________________
Fig. 2
Démarche diagnostique devant un goitre.
(Source : CEEDMM, 2021.)
________________________________________________________________________________
Les goitres peuvent être découverts par le patient, l’entourage, le médecin lors d’une consultation ou fortuitement lors d’un examen d’imagerie (échographie ou scanner). La démarche diagnostique doit permettre d’évaluer les caractéristiques du goitre, de rechercher d’éventuelles complications et d’éliminer une authentique pathologie thyroïdienne dont le goitre peut être la première manifestation.
A Interrogatoire
Il précise les antécédents familiaux de maladie thyroïdienne, l’existence d’une gêne fonctionnelle (déglutition, respiratoire) ou d’éventuels symptômes de dysthyroïdie.
B Examen clinique
La palpation cervicale retrouve l’hypertrophie thyroïdienne ascensionnant à la déglutition, apprécie l’importance du goitre, son caractère homogène ou non, la présence éventuelle d’adénopathies. Il faut rechercher le caractère plongeant du goitre, que l’on suspecte lorsque le pôle inférieur des lobes n’est pas perçu lors de la déglutition. On recherche des signes de dysthyroïdie (hyperthyroïdie ou hypothyroïdie).
C Biologie
- En première intention : dosage de la TSH.
- En deuxième intention, si la TSH est anormale :
- dosage de T4 pour quantifier l’importance de la dysfonction hormonale ;
- si TSH augmentée, dosage des anticorps anti-thyroperoxydases ou anti-thyroglobine (en cas de négativité des anticorps anti-TPO) à la recherche d’une thyroïdite auto-immune de Hashimoto ;
- si TSH basse, suivant le contexte :
- goitre diffus, sujet jeune : dosage des anticorps anti-récepteurs de la TSH pour éliminer une maladie de Basedow ;
- goitre plurinodulaire : scintigraphie thyroïdienne à la recherche d’un goitre multinodulaire toxique.
D Échographie thyroïdienne
Surtout utile lorsque le goitre est irrégulier, à la recherche de nodules, elle permet aussi d’apprécier l’aspect du parenchyme à la recherche d’une thyroïdite (aspect hypoéchogène), de mesurer le volume du goitre et de suivre son évolution. Il s’agit d’un examen opérateur-dépendant.
V Diagnostic étiologique
Dans l’immense majorité des cas, il s’agit d’un goitre simple pouvant avoir évolué vers une forme multinodulaire. Ce terme désigne les hypertrophies de la thyroïde normofonctionnelles (sans hyperthyroïdie ni hypothyroïdie), non inflammatoires (pas de thyroïdite), débutant généralement à l’adolescence mais pouvant être diagnostiquées plus tardivement.
Initialement, l’hypertrophie est diffuse et homogène (fig. 3), le plus souvent modérée. Le parenchyme est souple, régulier. La TSH est normale et les anticorps antithyroïdiens négatifs permettent d’exclure une thyroïdite auto-immunitaire ou une maladie de Basedow.
________________________________________________________________________________
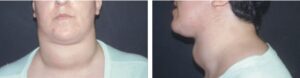
Fig. 3
Goitre diffus.
(Source : CEEDMM, 2021.)
________________________________________________________________________________
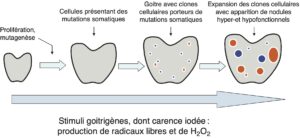
Au fil des années et des décennies, le goitre se remanie et certaines cellules acquièrent des mutations activatrices ou oncogéniques conduisant à l’apparition de nodules fonctionnels et de nodules non fonctionnels (fig. 4). C’est au stade de goitre plurinodulaire (fig. 5) qu’apparaît le risque de complications liées principalement au volume du goitre (risque de compression), au risque d’autonomisation progressive due aux nodules hyperfonctionnels (hyperthyroïdie), de survenue d’un cancer (nodules non fonctionnels).
________________________________________________________________________________
Fig. 4
Hypothèse de transformation nodulaire d’un goitre.
(Source : CEEDMM, 2021.)
________________________________________________________________________________
________________________________________________________________________________
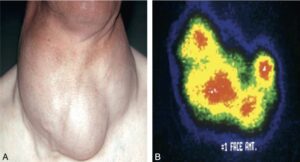
Fig. 5
Goitre multinodulaire autonomisé.
A. Goitre multinodulaire. TSH basse. B. Scintigraphie. Zones « chaudes » liées à des nodules hyperfonctionnels.
(Source : CEEDMM, 2021.)
________________________________________________________________________________
A Principaux risques évolutifs d’un goitre
1 Hyperthyroïdie
En raison de l’augmentation progressive de volume des nodules hyperfonctionnels, le goitre s’autonomise avec survenue d’une hyperthyroïdie qui reste longtemps fruste (TSH basse, dosages de T4 et T3 normaux) puis évolue vers la thyrotoxicose avec risque de complications cardiaques. La scintigraphie retrouve une alternance de plages fixantes et hypofixantes confirmant le goitre multinodulaire toxique. Il s’agit de la première cause d’hyperthyroïdie chez le sujet âgé. Le passage en hyperthyroïdie peut être déclenché par une injection iodée lors d’un scanner par exemple. Il n’est pas rare que des manifestations cardiaques (troubles du rythme à type de fibrillation auriculaire, insuffisance cardiaque) révèlent un goitre autonomisé méconnu (cf. Item 242 – Hyperthyroïdie).
2 Compression des organes de voisinage
Elle se marque par des troubles de la déglutition, une gêne respiratoire, plus rarement des signes de compression veineuse (turgescence jugulaire, circulation collatérale). À l’échographie, la partie basse du goitre n’est pas visualisée. La radiographie du thorax retrouve un élargissement du médiastin supérieur et une déviation trachéale (fig. 6), mais des informations plus précises sont données par le scanner (fig. 7) ou l’IRM, qui seront toujours demandés par le chirurgien en préopératoire. La scintigraphie thyroïdienne peut aider à apprécier l’importance du prolongement médiastinal.
________________________________________________________________________________
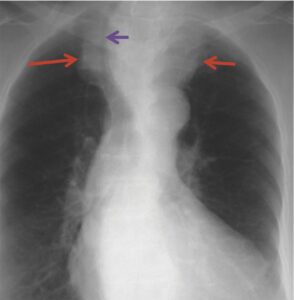
Fig. 6
Radiographie de trachée montrant un élargissement du médiastin supérieur (flèches rouges) et une déviation trachéale (flèche violette) sous l’effet d’un goitre plongeant.
(Source : CEEDMM, 2021.)
________________________________________________________________________________
________________________________________________________________________________
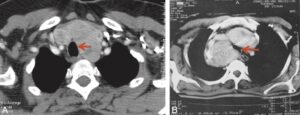
Fig. 7
Scanner cervicothoracique à la recherche d’une compression trachéale.
A. Déviation trachéale sans diminution du calibre trachéal (flèche). B. Volumineux goitre comprimant la trachée (flèche).
(Source : CEEDMM, 2021.)
________________________________________________________________________________
3 Cancer thyroïdien
Un cancer thyroïdien est présent dans 4 à 5 % des goitres plurinodulaires. Les nodules suspects à l’échographie doivent bénéficier d’une cytoponction (cf. infra, section « Nodules thyroïdiens »).
B Principales causes de goitre
1 Maladie de Basedow
Le diagnostic est le plus souvent évoqué chez une femme jeune, présentant un goitre diffus, une hyperthyroïdie, associée à d’éventuels signes extrathyroïdiens (orbitopathie). Le dosage des anticorps anti-récepteurs de la TSH confirme le diagnostic.
2 Thyroïdite subaiguë de De Quervain
Le début est brutal, le goitre est douloureux, très ferme, souvent irrégulier avec des signes biologiques d’inflammation (augmentation de la protéine C-réactive). Une hyperthyroïdie transitoire est possible par lyse cellulaire (relargage des hormones thyroïdiennes préformées, stockées dans la colloïde).
3 Thyroïdite auto-immunitaire de Hashimoto
Elle est caractérisée par l’association d’un goitre, d’une hypothyroïdie et d’anticorps antithyroïdiens à un titre élevé : anticorps anti-peroxydase (TPO) et/ou anti-thyroglobuline (Tg).
4 Autres causes
Les autres causes sont exceptionnelles :
- trouble de l’hormonosynthèse en relation avec diverses anomalies moléculaires (transporteur de l’iode, TPO, deshalogénase, pendrine, Tg). Le diagnostic est évoqué par le contexte familial, l’ancienneté du goitre depuis la petite enfance avec souvent hypothyroïdie congénitale ;
- sécrétion inappropriée de TSH : la TSH normale ou modérément augmentée s’accompagne de dosages de T4 et T3élevés. Cette discordance biologique peut être liée à un adénome thyréotrope ou un syndrome de résistance aux hormones thyroïdiennes (cf. Item 242 – Hyperthyroïdie).
VI Prise en charge thérapeutique
Le meilleur traitement (fig. 8) est la prévention par apport iodé suffisant pendant l’adolescence et la grossesse. L’intérêt d’un traitement thyroxinique au stade de goitre simple ou pendant la grossesse est discuté. Au stade de goitre nodulaire, les lésions sont irréversibles et les traitements thyroxiniques contre-indiqués car ils peuvent entraîner une hyperthyroïdie, le goitre étant, le plus souvent, déjà partiellement autonome.
________________________________________________________________________________
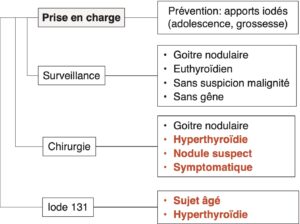
Fig. 8
Prise en charge des goitres.
(Source : CEEDMM, 2021.)
________________________________________________________________________________
Les goitres multinodulaires euthyroïdiens, non compressifs, sans suspicion de malignité peuvent bénéficier d’une surveillance. Dès que les goitres deviennent symptomatiques (gêne cervicale), en cas d’évolution vers une hyperthyroïdie ou de nodule thyroïdien suspect, il faut envisager un traitement radical, le plus souvent chirurgical. L’alternative, en cas d’hyperthyroïdie, chez un sujet âgé ou en mauvais état général est l’administration d’une dose thérapeutique d’iode 131, qui a l’avantage d’être un traitement non invasif, très efficace pour la correction de l’hyperthyroïdie, et de permettre aussi d’obtenir une réduction du volume du goitre de l’ordre de 30 à 40 %. Une préparation médicamenteuse par antithyroïdiens de synthèse est recommandée en cas d’hyperthyroïdie, avant la chirurgie ou l’administration d’iode radioactif, pour améliorer l’état général du patient et faciliter la tolérance du traitement. Avant toute décision thérapeutique, les diverses possibilités de prise en charge thérapeutiques ou de surveillance sont présentées au patient et discutées au cas par cas.
________________________________________________________________________________
________________________________________________________________________________
Points-clés
- Les goitres diffus homogènes s’organisent au fil des décennies en goitres plurinodulaires.
- Au stade plurinodulaire, les goitres peuvent être responsables de complications : compression locale, hyperthyroïdie, cancer thyroïdien.
- Le dosage de la TSH est l’examen de première intention.
- Beaucoup des goitres simples de l’adulte peuvent bénéficier de la seule surveillance. La chirurgie des goitres est particulièrement indiquée pour les goitres symptomatiques, hyperfonctionnels ou morphologiquement suspects.
- L’iode 131 constitue une alternative thérapeutique pour les goitres compressifs, hyperfonctionnels des sujets âgés et fragiles.
________________________________________________________________________________
© CEEDMM – Août 2022.
